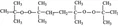Peroxide beziehen sich auf Verbindungen, die aus Sauerstoff und anderen Elementen gebildet werden, wobei Sauerstoff die Ladung -2 trägt. Aus der chemischen Formel geht hervor, dass sowohl Peroxide als auch Oxide Sauerstoff enthalten, ihre Ladungszustände von Sauerstoff sind jedoch unterschiedlich. Das Sauerstoffelement im Oxid hat eine Ladung von -2, während das Sauerstoffelement im Peroxid eine Ladung von -1 hat.
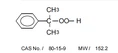
Peroxid bezieht sich auf ein Oxid, das zwei Sauerstoffatome enthält, wobei das Sauerstoffelement eine Ladung von -1 trägt. Zum Beispiel Wasserstoffperoxid, Benzoylperoxid usw. Oxide werden hauptsächlich zur Herstellung anderer Verbindungen oder als anorganische Materialien verwendet, während Peroxide und Oxide zwei verschiedene Verbindungen mit unterschiedlichen chemischen Eigenschaften, Strukturen und Verwendungszwecken sind.
1. Unterschiedliche Struktur: Die chemische Bindung zwischen den beiden im Peroxid enthaltenen Sauerstoffatomen ist entspannter und lässt sich leichter aufbrechen als die chemische Bindung zwischen den Sauerstoffatomen im Oxid, sodass die Zersetzungsgeschwindigkeit des Peroxids schneller ist als die des Oxids.
2. Unterschiedliche chemische Eigenschaften: Peroxide haben aktivere chemische Eigenschaften als Oxide, zersetzen sich leicht unter Bildung freier Radikale und haben starke oxidierende und reduzierende Eigenschaften. Beispielsweise kann Wasserstoffperoxid mit Metallen unter Bildung von Sauerstoff und Wasser reagieren. Obwohl sie alle Sauerstoff enthalten, ist der Ladungszustand des Sauerstoffs unterschiedlich und daher sind auch ihre Eigenschaften unterschiedlich. Obwohl Peroxide und Oxide Ähnlichkeiten aufweisen, handelt es sich daher um zwei unterschiedliche Verbindungen.
3. Verschiedene Verwendungsmöglichkeiten: Peroxide haben starke oxidierende und reduzierende Eigenschaften und werden häufig in der Bleich-, Desinfektions-, Oxidationsmittel- und anderen Bereichen eingesetzt. Zum Beispiel Eisenoxid, Zinkoxid usw.